19.2.4
Quand l’hépatite B se chronicise
Ibrahim, 32 ans, originaire du Cameroun, vous consulte car il est inquiet, il vient d’apprendre que sa mère et son frère aîné sont atteints de l’hépatite B. Il désire en savoir plus sur cette maladie et, surtout, s’il en est atteint lui aussi.
Vous recherchez rapidement dans le dossier patient d’Ibrahim une sérologie d’hépatite B et vous tombez sur ce résultat :

Introduction
Les dernières décennies ont mené à plusieurs avancées scientifiques dans le domaine de la santé, et plus précisément dans l’évolution des connaissances sur les hépatites virales. Ces progrès ont permis d’améliorer la santé populationnelle en dépistant, prévenant et traitant les différentes complications associées aux hépatites virales. Actuellement, il existe cinq types d’hépatites virales, soit l’hépatite A, B, C, D et E. Depuis plusieurs années, la prévention vaccinale contre l’hépatite A et B est disponible, mais demeure sous-utilisée dans certaines régions du monde.
L’hépatite B est un virus à ADN atteignant le foie et pouvant causer une infection virale aiguë ou chronique. Dans sa chronicité, l’infection par l’hépatite B représente un fardeau important pour les individus et les systèmes de la santé dans le monde, et le Canada n’en fait pas exception.
Au niveau mondial
En 2021, le Canada estimait le nombre de personnes atteintes par le virus de l’hépatite B (VHB) à 262 000 et seulement 58% de celles-ci avaient été diagnostiquées (Government of Canada, 2024). En 2022, uniquement 13% des 254 millions de personnes atteintes mondialement avaient reçu un diagnostic formel. Parallèlement, l’Organisation mondiale de la santé (OMS) estimait le nombre de décès liés à l’hépatite B à 1,1 million (WHO, 2024).
En 2022, les plus hauts taux de prévalence de l’hépatite B se situaient dans les régions sous-développées, comme le Pacifique occidental et l’Afrique, qui à elle seule, comptait 63% des nouvelles infections. Malgré ce pourcentage élevé, seulement 18% des nouveau-nés avaient bénéficié de la vaccination à la naissance (WHO, 2024).
Ces statistiques sont alarmantes et démontrent le sous-diagnostic de cette infection virale et la pertinence d’augmenter son dépistage. L’OMS travaille activement à mettre en place des stratégies mondiales dans le secteur de la santé afin de répondre à l’objectif d’éradiquer les hépatites virales d’ici 2030.
Modes de transmission
La transmission verticale (c’est-à-dire, de la mère infectée à son bébé durant la grossesse ou à la naissance) demeure le mode de propagation le plus fréquent. Les autres modes de transmissions sont respectivement le contact percutané avec du sang contaminé (aiguille, piqûre accidentelle, partage de seringues, rasoirs), le contact d’une muqueuse avec du sang, du sperme ou du liquide biologique contaminé ou, plus rarement, par transplantation d’organes ou de cellules souches.
L’infection peut être aiguë (durée de moins de 6 mois) ou chronique (durée de plus de 6 mois). La transmission en bas âge augmente significativement le risque de chronicisation. Ainsi, dans le cas d’une infection à la naissance, 90% évolueront vers une hépatite B chronique alors que ce pourcentage diminue à 25-50% si la transmission se fait avant l’âge de 5 ans et à 5% si elle est transmise à l’âge adulte (Institut national de santé publique du Québec [INSPQ], 2024).
Tableau clinique de la maladie
Dans la majorité des cas, qu’elle soit aiguë ou chronique, l’hépatite B reste asymptomatique. En phase aiguë, elle peut entraîner, notamment, de la nausée, de l’ictère, une hépatalgie ou encore de la fièvre. Le risque principal associé à l’hépatite B chronique demeure le développement d’une fibrose hépatique extensive, soit une cirrhose, ou d’un carcinome hépatocellulaire (CHC).
Différents facteurs de risques contribuent au développement d’un CHC chez cette clientèle, entre autres, l’âge et le sexe, la charge virale du VHB, la présence d’un antigène Hbs quantitatif élevé, le génotype viral du VHB (principalement A1, C, F), les expositions environnementales, les facteurs génétiques, les co-infections virales et l’ethnie (Osiowy & al, 2025).
L’infection souvent silencieuse, son faible taux de dépistage et les lacunes en matière de prévention et de promotion de la santé augmentent la mortalité et la morbidité au niveau mondial.
Vaccination et dépistage
La vaccination pour prévenir la transmission du virus a permis une nette diminution du taux d’infection par l’hépatite B au Québec et au Canada. Depuis 1994, la vaccination contre l’hépatite B est offerte aux élèves du primaire et elle est désormais intégrée dans le Programme d’Immunisation québécois (PIQ) (ministère de la Santé et des Services sociaux [MSSSS], 2024), ce qui diminue la prévalence de cette infection au Québec. Mondialement, le niveau de prévention varie, et ce, malgré la disponibilité du vaccin, ce qui contribue à la persistance de l’infection, notamment chez la clientèle issue de l’immigration.
Pour appuyer l’OMS dans sa mission d’éliminer le VHB au niveau mondial, tous les individus de plus de 18 ans devraient avoir minimalement une sérologie de dépistage pour l’hépatite B (Ag Hbs et anti-Hbc) au cours de leur vie, et plus périodiquement (Ag Hbs seulement) lorsque la personne présente des risques persistants à une nouvelle contamination (EASL, 2025). Les conditions supplémentaires nécessitant un nouveau dépistage sont présentées dans le Tableau 1.
Tableau 1 : Individus à dépister pour l’hépatite B (EASL, 2025)

La vaccination devrait être proposée d’emblée lorsque l’on constate un statut non vaccinal lors d’une sérologie pour l’hépatite B. La vérification du développement des anticorps post-vaccinaux n’est pas indiquée dans la pratique courante, sauf pour certains cas particuliers, comme les nouveau-nés de mère Ag HBs positive, les personnes pouvant présenter une réponse sous-optimale au vaccin, les personnes présentant un risque répété d’exposition au VHB, etc. (MSSS, 2024).
Interprétation de la sérologie
L’interprétation adéquate de la sérologie de l’hépatite B (Tableaux 2 et 3) permet d’identifier les personnes qui devraient bénéficier d’un suivi ou encore d’une vaccination.
Tableau 2 : Marqueurs sérologiques et interprétation
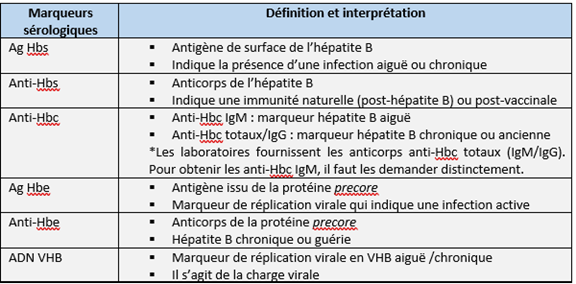
*La période fenêtre (moment entre l’exposition au virus et le premier marqueur sérologique détectable [Ag Hbs]) se situe entre une et douze semaines.
Tableau 3 : Interprétation des résultats et conduite
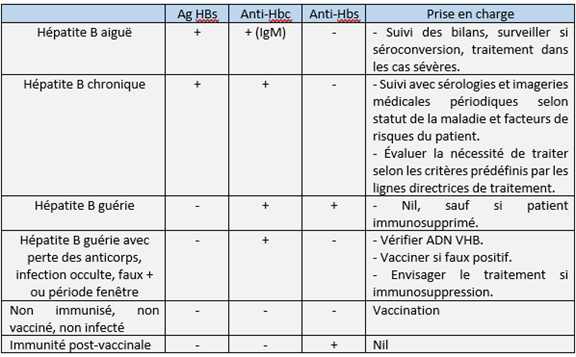
Tableau 4 : Interprétation des stades du VHB chronique (inspiré de EASL, 2025)
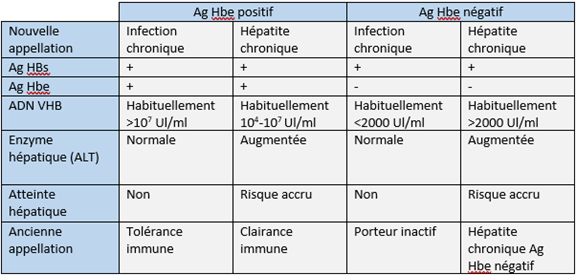
* On distingue l’infection chronique de l’hépatite chronique principalement par le risque d’atteinte hépatique.
Suivi d’une personne atteinte du VHB chronique
Les personnes atteintes par l’hépatite B chronique doivent avoir minimalement un suivi annuel. Les différents modes de transmission et de prévention ainsi que les complications doivent être divulguées clairement au patient et à sa famille. Le tableau 5 décrit des actions concrètes visant à limiter la propagation du virus. Il est impératif de sensibiliser les personnes atteintes d’avoir une observance exemplaire aux suivis et aux bilans sanguins afin de prévenir les complications en lien avec l’hépatite B. La vaccination contre l’hépatite A, l’influenza et le pneumocoque est fortement recommandée à cette clientèle.
Les facteurs de risques concomitants favorisant le développement d’une maladie hépatique surajoutée doivent également être abordés. La consommation d’alcool et les habitudes de vie prédisposant à un syndrome métabolique devraient être contrôlées et limitées.
Tableau 5 : Actions concrètes visant la prévention du VHB (Gouvernement du Canada, 2025)

Le suivi minimal comprend des bilans sanguins aux 6 à 12 mois, incluant la sérologie complète de l’hépatite B, la quantification de la charge virale, une formule sanguine ainsi qu’un bilan hépatique complet. Au diagnostic, il est important de s’assurer de l’absence d’une co-infection avec l’hépatite C et D, de même que pour le VIH. Une évaluation de la fibrose et une imagerie hépatique doivent être réalisées lorsqu’un diagnostic de VHB est posé.
L’évaluation du degré de fibrose par méthode non invasive devrait être privilégiée à la biopsie. Les scores non invasifs de fibrose, comme le FIB-4, le APRI et le FibroTest permettent d’évaluer facilement et rapidement le risque de fibrose hépatique à l’aide des bilans sanguins. Cependant, le Fibroscan (élastographie transitoire contrôlée par vibrations) reste une méthode bien plus précise permettant d’évaluer l’élasticité hépatique à l’aide d’une onde de cisaillement. L’imagerie par impulsion de force de rayonnement acoustique est une méthode semblable au Fibroscan qui nécessite un appareil d’échographie. Elle est de plus en plus disponible dans les services radiologiques. Ces deux différentes méthodes permettent d’obtenir la rigidité hépatique en kilopascals afin d’établir un stade de fibrose hépatique entre 0 (absence de fibrose) et 4 (fibrose extensive/cirrhose) (EASL, 2025).
Les personnes à risque de développer un CHC (clientèle décrite ci-bas) doivent avoir une imagerie (prioriser l’échographie pour le dépistage) bi- annuellement. La sérologie de l’alpha-foetoprotéine peut être utilisée en complément de l’imagerie dans le dépistage du CHC (Osiowy, 2025).
Clientèle VHB chronique à risque de développer un CHC :
- Tous patients ayant une cirrhose (Child Pugh A ou B, et C : imagerie seulement si en attente d’une greffe hépatique)
- Patients AgHBs + à risque élevé de CHC :
- Hommes ≥ 40 ans;
- Femmes ≥ 50 ans;
- Personnes d’origine africaine (noire) ≥ 30 ans;
- Histoire familiale au premier degré de CHC (à partir de 40 ans ou 10 ans avant le membre de la famille du premier degré affecté);
- Personnes co-infectées par l’hépatite Delta (à partir de 40 ans ou plus tôt si fibrose avancée >F3);
- Personnes co-infectées par le VIH (à partir de 40 ans)
Suivi d’une femme enceinte atteinte du VHB
Les femmes enceintes doivent avoir une surveillance biochimique plus étroite vu le risque augmenté d’activation du virus durant la grossesse. Des bilans sanguins incluant une sérologie complète de l’hépatite B (ADN VHB, Ag Hbe, anti-Hbe, Ag Hbs) et un bilan hépatique doivent être réalisés tous les trimestres de la grossesse et jusqu’à 6 mois post-partum (Osiowy, 2025; Terrault & al., 2018). L’ADN VHB doit être vérifié entre la semaine 28 et 32 pour déterminer si l’initiation d’un traitement est nécessaire (L. Badell & al., 2024). Une charge virale >200 000 UI/ml est une indication de débuter un traitement antiviral, idéalement avant le troisième trimestre pour limiter le risque de transmission du virus au bébé à naître (EASL, 2025). L’allaitement n’est pas contre-indiqué chez cette clientèle.
Quelques mots sur l’hépatite Delta
L’hépatite Delta est une infection hépatique qui nécessite le virus de l’hépatite B pour se répliquer. Elle touche 4 à 5% des VHB à l’échelle mondiale (EASL, 2025). La co-infection VHB/VHD représente la forme la plus grave d’hépatite virale, puisqu’elle a tendance à se compliquer plus rapidement vers la fibrose et le CHC. L’hépatite Delta doit être recherchée à l’aide des anticorps Anti-VHD chez tous les patients ayant un nouveau diagnostic de VHB. En présence d’anticorps anti-VHD positifs, il faut rechercher l’ARN VHD pour préciser s’il s’agit d’une infection active ou non. Il n’est pas nécessaire de répéter la sérologie anti-VHD lorsqu’elle s’avère négative, sauf en présence d’une nouvelle activité ou risque persistant pour le VHD ou d’une nouvelle élévation des enzymes hépatiques avec une charge virale du VHB <2000 UL/ml (Osiowy, 2025).
Retour sur le cas clinique d’Ibrahim.


Références
- Comberg, M., Sandmann L., Jaroszewicz, J., Kenedy, P., Lampertico, P., Lemoine, M., Lens, S., Testoni, B., Lai-Hung Wong, G., Paolo Russo, F. (2025) European Association for the Study of the Liver. EASL Clinical Practice Guidelines on the management of hepatitis B virus infection. .Journal of hepatology, 79, 502-583. https://doi.org/10.1016/j.jhep.2025.03.018
- Government of Canada. (2024). Canada's progress towards eliminating viral hepatitis as a public health threat.
https://www.canada.ca/en/public-health/services/publications/diseases-conditions/progress-towards-eliminating-viral-hepatitis-threat-2021.html - Gouvernement du Canada. (2025). Hépatite B: Prévention et risques.
https://www.canada.ca/fr/sante-publique/services/maladies/hepatite-b/prevention-risques.html - Institut national de santé publique du Québec. (2024). L’hépatite B. https://www.inspq.qc.ca/sante-voyage/guide/immunisation/hepatite-b
- Badell, M., Prabhu, M, T. N. Tita, A, S. Silverman, N. (2024). Socyety for Maternal-Fetal Medicine. Consult Series #69: Hepatitis B in pregnancy: update guidelines. American Journal of Obstetrics & Gynecology, 230, Issue 4, PB2-PB4.
https://www.ajog.org/article/S0002-9378(23)02173-7/fulltext - Ministère de la santé et des services sociaux. (2024). Vaccination contre l’hépatite B.
https://www.msss.gouv.qc.ca/professionnels/vaccination/piq-vaccins/hb-vaccin-contre-l-hepatite-b/#indications - Osiowy, C., Alvarez, F., S. Coffin, C., L. Cooper, C., F. Fung, S., Hin Ko, H., Poulin, S., van Gennip, J. (2025). La prise en charge de l’hépatite B chronique: mise à jour 2025 des lignes directrices de l’Association canadienne pour l’étude du foie et de l’Association pour la microbiologie médicale et l’infectiologie Canada. Canadian Liver Journal, 8(2). doi:10.3138/canlivj-2025-0012-f
https://utppublishing.com/doi/10.3138/canlivj-2025-0012-e - Terrault, N.A, Lok, A.S, McMahon, B.J., Chang, K.M., Hwang, J.P., Jonas, M.M., Brown Jr, R.S, Bzowej, N.H. & Wong, J.B. (2018). Update on Prevention, Diagnosis, and Treatment and of Chronic Hepatitis B: AASLD 2018 Hepatitis B Guidance. Hepatology, 67(4): 1560–1599. doi:10.1002/hep.29800.
https://pmc.ncbi.nlm.nih.gov/articles/PMC5975958/
- World Health Organization. (2024). Global hepatitis report 2024, Action for access in low-and middle-income countries. https://www.who.int/publications/i/item/9789240091672
Auteure
Par Valérie Bazin, IPSSA en Hépatologie, CHU de Québec
Citation
Bazin, V. (2025, décembre). Quand l’hépatite B se chronicise. Revue de l’AIPSQ.
